Вступ
Поліпшення лікування артеріальної гіпертензії (АГ) залишається важливою проблемою сучасної медицини. Після впровадження європейських рекомендацій 2018 року застосування фіксованої комбінації як старту лікування АГ для більшості пацієнтів стало важливим стандартом (2018-ESC/ESH). Такий підхід визнано основним і в інших більш сучасних настановах (2020-Global, 2023-ESH). Протягом останніх років на ринку України наявні подвійні та потрійні фіксовані комбінації від вітчизняних виробників. У травні 2009 р. FDA схвалило першу потрійну комбінацію амлодипіну, валсартану і гідрохлортіазиду в одній таблетці.
У наших попередніх публікаціях ми навели дані дослідження ТРИМАРАН як приклад ефективного застосування фіксованих комбінацій вітчизняного виробництва [1, 2]. У цьому дослідженні на основі аналізу даних 50 пацієнтів із 2–3-м ступенем підвищення АТ, яких лікували в академічних центрах, було показано ефективне та безпечне досягнення цільового артеріального тиску за допомогою фіксованої комбінації валсартану із амлодипіном та валсартану, амлодипіну та гідрохлортіазиду. Його тривалість (6 місяців) була достатньою для визначення антигіпертензивного ефекту та впливу на зміни органів-мішеней, але була недостатньою для оцінки ефекту на розвиток більш жорстких кінцевих точок — серцево-судинних ускладнень, госпіталізації, смерті та інших подій. Звісно, що прихильність до лікування протягом такого короткого періоду спостереження була високою. Тим не менш із літератури та практики відомо, що при довготривалому спостереженні (більше ніж рік) пацієнти часто відмовляються від лікування або замінюють його на інші препарати. Так, за даними наших попередніх досліджень, більше ніж 70 % хворих на АГ змінюють лікування протягом першого року [34]. Застосування подвійних та потрійних фіксованих комбінацій із самого початку лікування, імовірно, може зменшити частку таких пацієнтів при тривалому багаторічному спостереженні [13], але таких досліджень в Україні не проводилося.
Метою нашої роботи став аналіз 5-річної прихильності хворих, включених у дослідження –ТРИМАРАН, та ефективність і безпечність тривалої антигіпертензивної терапії фіксованими комбінаціями вітчизняного виробника.
Матеріали та методи
У дослідження ТРИМАРАН було включено 50 пацієнтів із АГ 2–3-го ступеня за класифікацією ВООЗ, які проходили стаціонарне або амбулаторне лікування у відділенні симптоматичних гіпертензій ДУ «Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України. Критеріями включення у дослідження ТРИМАРАН були: вік 25–75 років, АГ ІІ стадії, рівень систолічного (САТ) та/або діастолічного (ДАТ) АТ ≥ 160/100 мм рт.ст., підписання пацієнтом інформованої згоди на участь у дослідженні. Клінічне дослідження ТРИМАРАН проводили згідно із Законом України «Про клінічні засоби» та за етичними принципами, що викладені в Гельсінській декларації, а також згідно з «Інструкцією з проведення клінічних досліджень та експертизи матеріалів при клінічних дослідженнях», що затверджена наказом МОЗ України від 01.11.2000 року.
Відповідно до протоколу всім пацієнтам в рамках дослідження ТРИМАРАН були проведені наступні дослідження: збір анамнезу, вимірювання маси тіла та росту, об’єктивне обстеження, вимірювання офісного САТ і ДАТ, частоти серцевих скорочень (ЧСС), біохімічне дослідження крові, загальноклінічні дослідження крові та сечі, електрокардіографія, ехокардіографічне обстеження, добове моніторування АТ (ДМАТ) з вимірюванням центрального АТ, визначення жорсткості судинної стінки за індексом CAVI, реєстрація побічних явищ. Усім пацієнтам проводилося визначення росту та маси тіла, розраховувався індекс маси тіла (ІМТ = маса (кг)/зріст (м2)). Діагноз надлишкової маси тіла або ожиріння встановлювали відповідно до критеріїв ВООЗ (1997): надлишкову масу тіла встановлювали при значенні ІМТ від 25 до 29,9 кг/м2, ожиріння I ступеня — ІМТ від 30 до 34,9 кг/м2, ожиріння II ступеня — ІМТ від 35 до 39,9 кг/м2, ожиріння III ступеня — ІМТ ≥ 40,0 кг/м2. Вимірювання АТ проводили на апараті Omron M10, Японія. Реєстрацію САТ і ДАТ у положенні сидячи проводили на одній і тій же руці два рази з інтервалом у дві хвилини, якщо величини АТ не різнилися більш як на 5 мм рт.ст. При виявленні більшої різниці між отриманими величинами проводили третє вимірювання та обчислювали середнє значення з двох або трьох послідовних вимірювань. ЧСС визначали після другого вимірювання.
ДМАТ проводили на портативному апараті АВРМ-04 («Медітек», Угорщина). Моніторування проводилось у наступному режимі: у денний час — кожні 15 хвилин, уночі (з 22.00 до 6.00) — кожні 30 хвилин. Хворим було рекомендовано звичайний спосіб життя з виконанням побутових фізичних і психоемоційних навантажень.
Жорсткість судинної стінки вимірювалась за допомогою приладу САVI (VaSera 1500, Fukuda Denshi, Японія), манжети накладалися на обидві руки та ноги в положенні лежачи й одночасно відбувалося вимірювання жорсткості судинної стінки [49].
Усім пацієнтам була призначена подвійна або потрійна фіксована комбінація валсартан/амлодипін або валсартан/амлодипін/гідрохлортіазид. Ми простежили за пацієнтами через 5 років після призначеного лікування. Провели офісне вимірювання АТ, ДМАТ, вимірювання маси тіла, визначення жорсткості судинної стінки за індексом CAVI.
Пацієнти були поділені на 2 групи методом конвертів по 25 у кожній. Першій групі (n = 25) було призначено препарат Комбісарт Н, фіксована потрійна комбінація, таблетки виробництва АТ «Київський вітамінний завод». Препарат призначався по 1 таблетці (160 мг валсартану/5 мг амлодипіну/12,5 мг гідрохлортіазиду) один раз на добу, вранці протягом 1 місяця. Препарат пацієнт мав приймати в один і той же час. Таблетки приймалися цілими, з невеликою кількістю рідини під час або одразу після прийому їжі.
Пацієнти другої групи (n = 25) отримували за аналогічною схемою подвійну фіксовану комбінацію — препарат Комбісарт виробництва АТ «Київський вітамінний завод». Препарат призначався по 1 таблетці (160 мг валсартану/5 мг амлодипіну) один раз на добу, вранці протягом 1 місяця. Препарат пацієнт мав приймати в один і той же час. Таблетки приймалися цілими, з невеликою кількістю рідини під час або одразу після прийому їжі.
Ми простежили за пацієнтами через 5 років та встановили, скільки пацієнтів залишилися на терапії, скільки змінили терапію, які виникли побічні явища та у скількох пацієнтів, як змінилася жорсткість артерій за індексом CAVI через 5 років на терапії.
Результати
Дослідження ТРИМАРАН показало, що при прийомі подвійної (на основі валсартану та амлодипіну) або потрійної (на основі валсартану, амлодипіну та гідрохлортіазиду) фіксованої комбінованої терапії відбувалося значне достовірне зниження артеріального тиску при добовому моніторуванні у пацієнтів із помірною та тяжкою артеріальною гіпертензією через 3 місяці терапії. На подвійній фіксованій комбінації (валсартан/амлодипін — препарат Комбісарт) зниження 24САТ/24ДАТ через 3 місяці становило 18,0/16,1 мм рт.ст. (р < 0,05); на потрійній фіксованій комбінації (валсартан/амлодипін/гідрохлортіазид — препарат Комбісарт Н) — 23,8/20,7 мм рт.ст. (р < 0,05). Досягнення цільового рівня АТ при ДМАТ становило на подвійній фіксованій комбінації Комбісарт (валсартан/амлодипін) 77,3 %, у групі Комбісарту Н (валсартан/амлодипін/гідрохлортіазид) — 95,2 %. Тобто через 3 місяці постійного прийому фіксованих комбінацій вдалося досягти цільового рівня АТ майже у всіх пацієнтів.
Через 5 років після закінчення основного дослідження нам вдалося зв’язатися із 40 пацієнтами (із 50), які початково були включені у дослідження ТРИМАРАН. Менша кількість пацієнтів на цьому етапі спостереження була обумовлена відомими факторами: пандемія COVID-19 (2020–2021 роки) та військовий стан (з 2022 року), коли певна частка хворих була вимушена або переїхати, або емігрувати, і зв’язок із ними було втрачено. Тільки 42 % (16 пацієнтів) залишилися на фіксованій комбінації Комбісарт/Комбісарт Н. 58 % (24 пацієнти) змінили терапію. Дані наведені на рис. 1. Із групи пацієнтів, що змінили терапію, 60 % перейшли на інші блокатори рецепторів ангіотензину II (БРА ІІ), а 40 % — на інгібітори ангіотензинперетворювального ферменту (АПФ).
Характеристики пацієнтів на етапі 5-річного спостереження наведені в табл. 1. Як видно із табл. 1, пацієнти, що перейшли на іншу терапію, були старші за віком, хоч і недостовірно (ймовірно, це пов’язано з невеликою кількістю пацієнтів) та мали достовірно вищий рівень офісного АТ порівняно з групою пацієнтів, що лишилися на фіксованій комбінації Комбісарт чи Комбісарт Н.
У результаті дослідження ми встановили, що досягнення цільового офісного АТ через 5 років становило 78 % у групі Комбісарту/Комбісарту Н та лише 25 % — у групі іншої терапії. За даними добового моніторування, у групі Комбісарту/Комбісарту Н досягнення цільового АТ становило 70 %, а в групі іншої терапії — лише 55,5 %. Дані наведені на рис. 2.
Оцінюючи зміни АТ при добовому моніторуванні, ми встановили, що пацієнти, які змінили терапію, мали достовірно вищі цифри АТ при ДМАТ: 24САТ/24ДАТ — 135,4/79,8 мм рт.ст. — порівняно з пацієнтами, що залишилися на фіксованій комбінації Комбісарт/Комбісарт Н — 123,7/78,4 мм рт.ст., що становило 11,7/1,4 мм рт.ст. (р < 0,05 для САТ). Дані наведені на рис. 3. Така сама динаміка була і за денний та за нічний періоди (139,0/83,7 проти 127,2/83,3 мм рт.ст., що становило 11,8/0,4 мм рт.ст., та 127,8/72,1 проти 114,6/71,4 мм рт.ст., що становило 13,2/0,7 мм рт.ст. (р < 0,05 для САТ).
У лікуванні пацієнтів із АГ важливим компонентом є вплив на ураження органів-мішеней. Так, ми оцінили жорсткість артерій за індексом CAVI, який не залежить від АТ, через 5 років терапії та виявили, що CAVI достовірно відрізнявся в групах лікування та був нижчим в групі Комбісарт/Комбісарт Н як справа, так і зліва: 8,79 проти 6,08 та 8,64 проти 6,28 відповідно (р < 0,05 для усіх значень). Тобто можна сказати, що фіксована комбінація у вигляді препаратів Комбісарт/Комбісарт Н сприяла зменшенню прогресування жорсткості артерій, окрім кращого контролю АТ. Дані наведені на рис. 4.
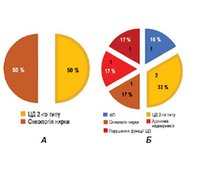
Ми оцінили розвиток комбінованої кінцевої точки у вигляді виникнення ІМ, ЦД, ГПМК, ФП, смерті тощо. Так, ми виявили, що у групі іншої терапії всього було 6 випадків кінцевих точок (2 нові випадки цукрового діабету 2-го типу, по 1 випадку фібриляції передсердь, онкології нирки, виявлення аденоми наднирників, порушення функції щитоподібної залози), а в групі фіксованої комбінації Комбісарт/Комбісарт Н лише 2 (випадок онкології нирки та розвиток цукрового діабету 2-го типу). Дані наведені в табл. 2 та на рис. 5. Тобто виявлена достовірна різниця в групах терапії з переважанням в 3 рази випадків розвитку комбінованої кінцевої точки в групі іншої терапії порівняно з фіксованою комбінацією Комбісарт/Комбісарт Н.
За оцінкою біохімічних показників ми не відмітили достовірної різниці в основних показниках між групами, окрім достовірно вищого рівня сечової кислоти в групі іншої терапії, що свідчить про те, що на фоні фіксованої комбінації Комбісарт/Комбісарт Н не спостерігалося підвищення рівня сечової кислоти, незважаючи на прийом гідрохлортіазиду, що входить до складу Комбісарту Н.
Обговорення
Дослідження ТРИМАРАН показало, що при прийомі подвійної (на основі валсартану та амлодипіну) або потрійної (на основі валсартану, амлодипіну та гідрохлортіазиду) фіксованої комбінованої терапії відбувалося значне достовірне зниження артеріального тиску при добовому моніторуванні у пацієнтів із помірною та тяжкою артеріальною гіпертензією через 3 місяці терапії. На подвійній фіксованій комбінації (валсартан/амлодипін — препарат Комбісарт) зниження 24САТ/24ДАТ через 3 місяці становило 18,0/16,1 мм рт.ст. (р < 0,05); на потрійній фіксованій комбінації (валсартан/амлодипін/гідрохлортіазид — препарат Комбісарт Н) — 23,8/20,7 мм рт.ст. (р < 0,05). Досягнення цільового рівня АТ при ДМАТ становило на подвійній фіксованій комбінації Комбісарт (валсартан/амлодипін) 77,3 %, у групі Комбісарту Н (валсартан/амлодипін/гідрохлортіазид) — 95,2 %. Тобто через 3 місяці постійного прийому фіксованих комбінацій вдалося досягти цільового рівня АТ майже у всіх пацієнтів.
Дані нашого дослідження збігаються з роботами авторів, які також довели переваги використання фіксованих комбінацій валсартан/амлодипін та валсартан/амлодипін/гідрохлортіазид щодо розвитку кінцевих точок та прогнозу. Так, метою дослідження Kyoto Heart Study було визначити вплив валсартану, який додавався до традиційної терапії пацієнтів з АГ високого ризику, на частоту розвитку ускладнень і смерті [34]. Первинна кінцева точка була комбінованою — фатальні або нефатальні кардіоваскулярні події. У дослідження був включений 3031 японський пацієнт (43 % — жінки, середній вік 66 років) з неконтрольованою артеріальною гіпертензією. Вони були рандомізовані приймати або валсартан, або лікування без БРА. Валсартан додавався до вже раніше призначеної терапії. Середній період спостереження становив 3,27 року. В обох групах вихідний АТ був 157/88 мм рт.ст., а в кінці спостереження — 133/76 мм рт.ст. У групі валсартану частота виникнення первинної кінцевої точки порівняно зі стандартною терапією була достовірно меншою (83 проти 155, співвідношення ризику 0,55, 95% ДІ 0,42–0,72, P = 0,00001). Крім того, спостерігалося достовірне зменшення частоти розвитку інсульту (співвідношення ризику 0,55, P = 0,015) і стенокардії (співвідношення ризику 0,51, P = 0,011), нових випадків цукрового діабету (Р = 0,028). Таким чином, додавання валсартану сприяло поліпшенню контролю АТ і запобігало виникненню кардіоваскулярних подій порівняно з традиційною терапією, що не може бути пояснено лише відмінностями в контролі артеріального тиску.
Проведений метааналіз 2023 року M. Xie et al. мав на меті оцінити ефективність комбінованих антигіпертензивних препаратів у пацієнтів із неконтрольованою АГ. Оцінювали лише рандомізовані контрольовані дослідження з ефективності комбінованих антигіпертензивних препаратів в одній таблетці у людей з неконтрольованою гіпертензією. Огляд включав 32 дослідження (16 273 пацієнти) з неконтрольованою АГ. Результати метааналізу показали, що було включено 11 комбінованих антигіпертензивних препаратів, а саме: амлодипін/валсартан, телмісартан/амлодипін, лозартан/гідрохлортіазид, кандесартан/гідрохлортіазид, амлодипін/беназеприл, телмісартан/гідрохлортіазид, валсартан/гідрохлортіазид, ірбесартан/амлодипін, амлодипін/лозартан, ірбесартан/гідрохлортіазид та периндоприл/амлодипін. Автори дійшли висновку, що комбінація БРА/БКК мала переваги порівняно з іншими фіксованими комбінаціями щодо впливу на САТ, ДАТ, швидкість контролю артеріального тиску [39].
D. Calhoun et al. протягом 8 тижнів лікували 2271 пацієнта з помірною гіпертензією потрійною (амлодипін/валсартан/гідрохлортіазид з титруванням дози до 10/320/25 мг) або подвійною комбінацією (амлодипін/валсартан, амлодипін/гідрохлортіазид, валсартан/гідрохлортіазид), досягнення цільових рівнів АТ відбулося в 71 % пацієнтів із потрійною терапією і у 45–54 % — із подвійною терапією [6, 7]. Це збігається з даними нашого дослідження: досягнення цільових рівнів АТ через 5 років на фоні фіксованої комбінації Комбісарт/Комбісарт Н становило 70 %.
Важливе значення серед метаболічних ефектів антигіпертензивних препаратів має обмін сечової кислоти, оскільки гіперурикемія асоціюється з АГ і є фактором ризику серцево-судинних захворювань. Так, підвищення рівня сечової кислоти в крові на 1 мг/дл можна порівняти за значимістю з підвищенням артеріального тиску на 10 мм рт.ст. Відомо, що лозартан має виражену урикозуричну дію. Вивчення ефектів валсартану на обмін сечової кислоти показало відсутність впливу на ниркову екскрецію сечової кислоти і рівень урикемії як у здорових добровольців, так і у пацієнтів із АГ [15–17]. Нові дані з вивчення механізмів впливу сартанів на обмін сечової кислоти були отримані в дослідженні з її транспортерами: валсартан і олмесартан показали здатність пригнічувати активність аніонного транспортера ОАТ3, який бере участь у канальцевій секреції сечової кислоти, а лозартан, телмісартан і кандесартан — здатність пригнічувати захоплення сечової кислоти через MRP4, причому лозартан це робить у найменших концентраціях. Що і було продемонстровано в нашому дослідженні, коли в групі Комбісарт/Комбісарт Н через 5 років терапії рівень сечової кислоти був достовірно нижчим порівняно з іншою терапією.
Погана прихильність до антигіпертензивної терапії є основною причиною поганого контролю АТ у пацієнтів з АГ. Спрощення схеми може поліпшити прихильність і контроль АТ. Системний метааналіз 2021 року 16 досліджень, у яких оцінювали прихильність, проведений Parati et al., показав, що у пацієнтів, які отримували фіксовану комбінацію, значно поліпшилася прихильність і була значно меншою ймовірність припинення терапії, ніж у пацієнтів, які отримували вільну комбінацію.
Обмеженням нашого дослідження є невелика кількість пацієнтів. Але метааналіз Cochrane 2024, проведений I. Toews et al., продемонстрував відсутність різниці між оцінками ефекту у великих рандомізованих клінічних дослідженнях та обсерваційних дослідженнях.
Довготривале спостереження за пацієнтами з тяжкою та помірною АГ в нашому дослідженні показало, що дотримання режиму лікування та прийом фіксованих комбінацій у вигляді Комбісарту та Комбісарту Н сприяє поліпшенню прихильності до лікування, кращому контролю АТ зі зменшенням розвитку комбінованих кінцевих точок та зменшенням прогресування ураження органів-мішеней у вигляді зниження жорсткості судинної стінки за індексом CAVI порівняно з групою зміненої терапії.
Висновки
1. Тривала 5-річна терапія фіксованими комбінаціями Комбісарт/Комбісарт Н була більш ефективна порівняно із іншою терапією у хворих із 2–3-м ступенем підвищення артеріального тиску.
2. Кількість комбінованих кінцевих точок при продовженні терапії Комбісартом/Комбісартом Н протягом 5 років була меншою порівняно з іншою терапією.
3. Жорсткість магістральних артерій за величиною індексу CAVI була достовірно меншою при тривалій терапії фіксованими комбінаціями Комбісарт/Комбісарт Н порівняно з іншою терапією.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 01.05.2024
Рецензовано/Revised 11.05.2024
Прийнято до друку/Accepted 21.05.2024

/19.jpg)
/20.jpg)
/21.jpg)